据悉,上海先博生物科技有限公司与江苏谱新生物医药有限公司已达成战略合作协议,委托谱新生物进行CAR-T药物二期注册临床及产品上市后商业化生产,这是国内已知的第一个基于MAH制度下的细胞产品商业化生产订单。
全球首款批准上市CAR-T药物
2017年8月31日,诺华(Novartis)宣布,美国FDA已经批准其CAR-T疗法上市,用于治疗B细胞前体急性淋巴性白血病(ALL),商品名为Kymriah。Kymriah的上市具有里程碑式的意义,标志着“活的药物”的商业化之路正式拉开帷幕,将加速更多细胞治疗产品的上市,造福肿瘤患者。
图片来源于网络
CAR-T药物首次登录中国市场
2021年,被称为中国细胞治疗药物商业化的元年。
2021年6月23日,复星凯特的阿基仑赛注射液于中国获批上市,该产品是国内首款正式获批的CAR-T产品,由Kite Pharma的Yescarta经过技术转移并进行本地化生产。
同年9月3日,药明巨诺的瑞基奥仑赛注射液于中国获批上市,该产品由药明巨诺自主研发,是中国首个获批为1类生物制品的CAR-T产品。
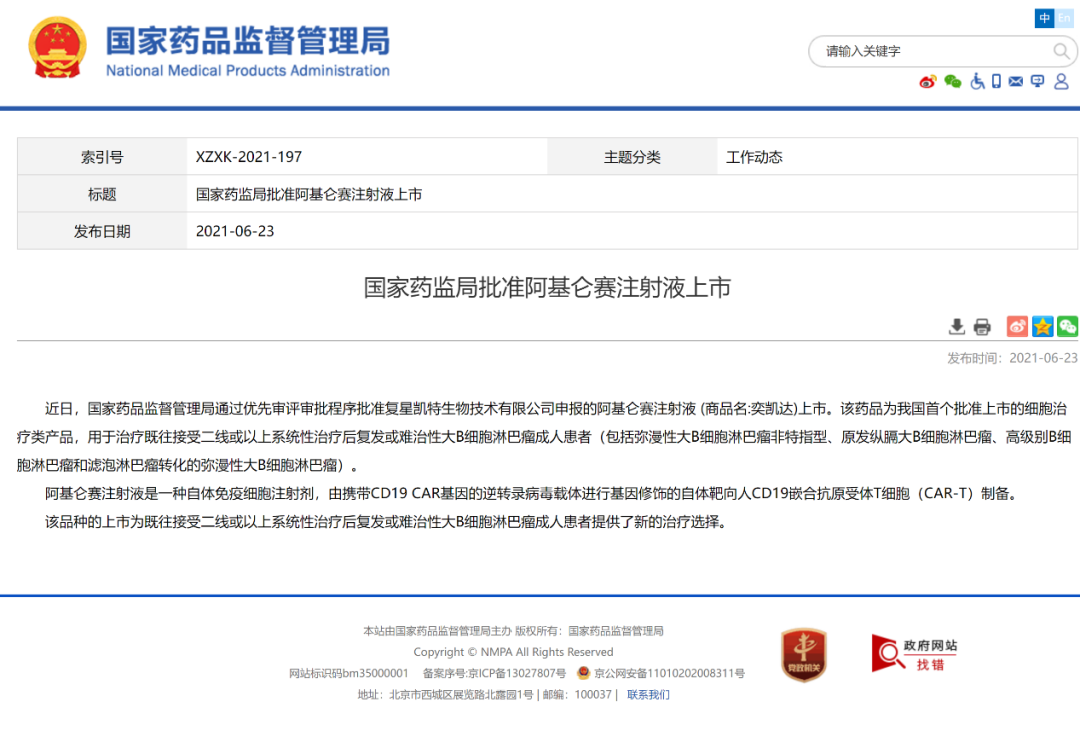
图片来源于国家药品监督管理局官网
回顾国内细胞治疗药物注册临床进度,截至2022年3月,CDE共受理135个细胞治疗产品的各类申请(自北京永泰的扩增活化的淋巴细胞申请临床算起,该产品已获批临床,之前受理的标准较低,未纳入统计)。其中绝大部分为试验性新药(IND)申请(包括8项补充申请),仅有3个为上市申请(目前已获批2个)。在这135个申请中,70个为CAR-T,25个为其他类型的免疫细胞治疗;31个为MSC,其他类型的前体细胞为9个。在132个临床申请中(包括近期受理、尚在审评中的品种),共有88个获批临床。
国内首个基于MAH制度下的
二期临床及商业化CAR-T订单
纵观国内已上市或准备上市CAR-T产品的商业化生产多为企业自建产能,在药品上市许可持有人(MAH)制度等国家利好政策支持下,国内生物制品企业也正不断探索新的合作发展模式。

据悉,先博生物与谱新生物已达成战略合作协议,委托谱新生物进行CAR-T药物二期临床及商业化生产,这是国内第一个基于MAH制度下的细胞生产商业化生产订单。作为专业、专注的细胞药物CDMO龙头,谱新生物正式叩开细胞药物领域全新合作模式的大门。
MAH制度与细胞药物的商业化之路
细胞治疗药物研发成本高,周期长,注册申报缺乏经验、产品个性化程度高、技术人才短缺、商业化生产能力薄弱等行业问题随着发展不断凸显并亟待解决,同时国内针对细胞治疗药物的法规多为征求意见稿等行业试点规范性制度,政策法规层面也亟待完善。
因此,对于研产一体的企业,从产品孵化到落地生产商业化全线的技术、管理及资金调配能力等挑战极大。如何持续提升生产品质、管控成本、合理配置投资将成为企业的关键课题,向CDMO企业“借力”不失为一种优质的选择方案,同时也优化了产业生态和助力长期可持续的发展。
MAH制度是将药品上市许可与药品生产许可进行分离,重置医药市场的各方“产能”,优化资源配置,让专业的机构干专业的事。MAH制度的发展,也催生出医药行业现在的高景气赛道CXO,如CRO、CMO、CDMO等一系列专业机构,特别是CDMO这种能为制药企业提供医药特别是创新药工艺研发、优化、放大、注册申报及商业化生产等服务的一站式的技术服务机构。
CDMO产业的健康发展,能够使得制药行业资源灵活调动并平衡,促进全球药物生产和流通合作,使得好药有生产,推进“全球药物+全球共享”模式。
放眼国际,CDMO能协助跨国制药公司在本土进行创新药物的研究和生产,这将极大帮助中国患者第一时间用上全球创新药物。
回看国内,CDMO产业将赋能中国生物初创企业,这些企业在推进研发成果乃至后续的优化及商业化生产过程中面临巨大挑战,成熟的CDMO企业可提供一站式的技术业务服务及全球网络供应链,不仅能够降低药物的研发生产成本,完整的供应链还能加速本土创新药物进入国际市场。
CDMO产业,将加速构建“全球创新药物+全球患者应用”的商业模式,提升药物的可及性和老百姓的可支付性,为全球患者带来获益。
实施MAH后,企业作为MAH持有人,对药品的非临床研究、临床试验、生产经营、上市后研究、不良反应监测及报告与处理等承担主体责任。那么选择“靠谱又专业”的受托机构就相当重要。专注特定产品领域、业务经营诚信、确保持续合规、拥有专业高素质人才团队、能有效提速受托方项目,在相关领域拥有丰富行业经验的受托机构无疑是上佳之选。
“21世纪,是细胞治疗的时代”,诺贝尔奖获得者詹姆斯·罗斯曼如是说。细胞治疗的时代已然到来。2022年,作为专注细胞药物解决方案提供商的谱新生物,陆续完成了超1亿元的融资。
诚如谱新生物CEO朱逸博士所说:
以 CAR-T 为代表的免疫细胞治疗产品已经在全球取得产业化成功。中国极有可能在未来的10 年内成为全球最大的细胞治疗市场。随着细胞药物品种的不断推陈出新,参与开发的企业和项目数量不断增加,对于专业细胞药物 CDMO 服务的需求也与日俱增。谱新生物致力于细胞药物的产业化,构建健康发展的产业生态,为广大病患能够更快更好地得到治疗并摆脱病患,贡献自己的一份力量。
正如谱新生物的公司愿景:让细胞药物谱写生命新篇章。期待更多如谱新生物这样优秀的CDMO企业助力细胞药物时代的飞速发展,让更多更好的细胞药物,更快的触及病患,推进全球药物共享,共同谱写细胞药物时代的新篇章!


Building 4, Yuewang Wisdom Valley, 1463 Wuzhong Avenue, Wuzhong District, Suzhou, China